ÖZET:
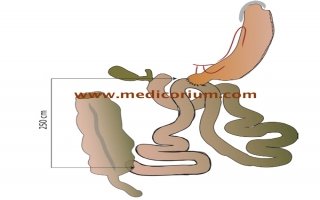
Tek Anastomozlu Duodenoİleal Bypass+Sleeve Gastrektomi basitleştirilmiş, 200-250 cm ortak kanal oluşturan, tek loop duodenal switch ameliyatıdır. Bu çalışmanın amacı ardışık olarak ameliyat edilen 100 vakada metabolik değişiklikler ve kilo kaybını analiz etmektir.
Çalışmaya kabul edilme kriterleri hastaların morbid obez veya metaboik hastalığa sahip olmalarıdır. İlk 50 hastada ortak kanal 200 cm olarak uygulanmış, sonraki vakalarda hipoproteinemi oranlarını düşürmek için 250 cm'de karar kılınmıştır.
Sonuçlar:
Seride ölüm veya ağır komplikasyon gözlenmemiştir. İzlem süresince ortalama EWL (fazla kilo kayıp oranı) % 95'in üzerindedir. Hastaların % 90'ından fazlasında Tip 2 diyabet tamamen düzelmiştir. Dirençli hipoproteinemi nedeniyle iki vakada daha uzun ortak kanal gerektiren standart duodenal switch'e geçilmiştir. Hipertansiyon vakaların % 98'inde kontrol altına alınmış, % 58'inde düzelmiştir. Ortalama defekasyon sayısı günde 2.5'tur.
Tartışma:
SADI-S (Tek Anastomozlu Duodenoİleal Bypass+Sleeve Gastrektomi) hem morbid obezite, hem de metabolik komplikasyonların tedavisinde çok iyi sonuçlar sunan, güvenli ve gerçekleştirilmesi daha hızlı olan basitleştirilmiş bir duodenal switch operasyonudur.
Biliopankreatik diversiyon (BPD) ve duodenal switch (BPD-DS) morbid obezite ve eşlik eden metaboik hastalıkları olan seçilmiş hastalarda uygun olabilecek cerrahi seçeneklerdir. (1-3) Bunlar teknik olarak oldukça kompleks operasyonlardır ve postoperatif komplikasyon oranları diğer obezite ameliyatlarından daha yüksektir. (3,4) Daha iyi kilo kaybı ve daha yüksek oranda metabolik düzelme sağlarlar (5), ancak gastrik bypass ve diğer kısıtlayıcı prosedürlere göre daha yüksek oranda protein ve vitamin eksikliklerine yol açarlar. (6,7)
Bu ameliyatların prensiplerini koruyarak tekniğini basitleştirmek üzere 2007'de SADI-S tekniği ileri sürülmüştür. (8,9) Bu ameliyat basitçe tek bir anastomoz, yani mide-barsak bileşimi içerir. Roux-en-Y anastomozları ortadan kalkmıştır. Çünkü mide çıkışında pylorun korunması, mide mukozasını safranın tahrişine karşı koruyarak safra saptırıcı işlemi gereksiz hale getirir. Başlangıçta, çekumdan, yani kalınbarsak-incebarsak bileşkesinden 200 cm mesafede bir duodenoileostomi yapılmıştır. Bu barsak uzunluğu beslenme bacağı için kısa, ortak kanal için çok uzundur.
Bazı hastalarda aşırı emilim bozukluğu geliştiği için, bacak uzunluğu 250 cm olarak revize edilmiştir. Sunulan 100 hastadan ilk 50'si 200 cm, sonraki 50'si 250 cm'den anastomoz yapılan hastalardır.
Metod:
Mayıs 2007'den Mayıs 2011'e kadar morbid obezite veya metabolik hastalıklar nedeniyle 100 hasta ameliyat edilmiştir. Bunlardan 93'ü primer operasyon, 7'si sleeve gastrektomiden sonra ikinci basamaktır. Kabul kriterleri BMI 40-50 arasında olması ve daha önce geçirilmiş bariatrik operasyon olmamasıdır. Başlangıç sonuçlarının yüz güldürücü olmasını takiben kriterler, obezite veya metabolik hastalıklar nedeniyle cerrahiye gönderilen tüm hastaları kapsayacak şekilde genişletilmiştir.
Ameliyat daha önce de tanımlanmıştır. (8,9) Mide büyük kurvaturunun devaskülarizasyonunu takiben, 54 F buji üzerinden bir sleeve gastrik rezeksiyon gerçekleştirilir. Duodenum gastroduodenal arterin altından disseke edilir ve 60 mm mavi kartuş lineer staplerle ayrılır. İleokolik bileşke bulunarak 250 cm proksimali hesaplanır. Barsak ölçümü, barsakları tamamen gevşetmek ve maksimum olası uzunluğu sağlamak için Buscopan enjeksiyonundan sonra, antimezenterik kenardan 10'ar cmlik tutuşlarla yapılır.
Seçilmiş loop antekolik ve yan-yana olacak şekilde proksimal duodenuma 30 mm lineer staplerle anastomoze edilir. Üst duvar 2 tabaka 000 vicryl sütürlerle kapatılır. Hasta oral gıda almaya başlayana kadar kalacak bir vakumlu dren yerleştirilir.
Ameliyat sonrası ilk ayda düşük kalorili, sıvı ve püreden ibaret bir diyet uygulanır. Multivitamin destekleri, kalsiyum ve demir preparatları kan tahlillerine göre destek olarak eklenebilir.
Sonuçlar:
Toplam 100 hastanın 63'ü kadın, 37'si erkek olup, yaş ortalaması 47 (22-71) idi. İlk prosedür olarak SADI uygulanan hastaların ortalama kilosu 119.5 (72-164), ortalama BMI değeri 44.6 (33-67) idi. Ortalama excess weight (fazla kilo) 53 kg (28-99) idi. İkincil operasyon olarak SADI uygulanan hastaların ortalama ameliyat öncesi ağırlığı 127 kg(94-160), ortalama BMI 48.5 (37.6-54.6) ve ortalama fazla kilosu 62 (31.5-84) kg idi.
100 hastadan 59'unun Tip 2 diyabeti vardı. Bunlardan 25'i (% 42) insülin tedavisi gerektirecek düzeyde diabetikti. Ortalama hastalık süresi 9.8 yıldı (0-30). Ameliyat öncesi ortalama kan şekeri düzeyi 178.2 (91-408), ortalama HbA1c düzeyi 7.9 (5.4-13) idi. Ortalama ameliyat öncesi C-peptid 2.12 (0.4-7) bulundu. Preoperatif dislipidemi hastaların 57'sinde, obestrüktif uyku apnesi 27'sinde ve hipertansiyon 57'sinde mevcuttu.
İlk 50 vakada duodenoileal anastomoz ileoçekal valvden 200 cm proksimalden yapıldı. Son 50 vakada bu uzunluk 250 cm'e çıkarıldı. Ameliyatların tümü laparoskopik gerçekleştirildi. Ancak daha önce geçirilmiş batın ameliyatı olan 3 vakadan birinde anastomozu gerçekleştirmedeki teknik güçlükler nedeniyle açık ameliyata geçildi.
İntraoperatif komplikasyon veya postoperatif yaşam kaybı görülmedi. Takip hastaların % 99'unda tamamlandı. Üç postoperatif kaçak saptandı. Bunlardan ikisi mide tüpünden, biri de duodenoileal anastomozdan gelişti. Tümü konservatif tedaviyle başarılı olarak kapandı. Bir vakada midede kanama gelişti ve endoskopik koagulasyonla tedavi edildi. Bir hastada akut trokar yeri fıtığı gelişti, tekrar operasyon ve meshle tamir uygulandı.
Fazla kilo kaybı (ideal 25 BMI'a göre hesaplandı) ilk 12 ayda % 95'e ulaştı. Takip eden yıllarda da korundu. SADI-200 ile SADI-250 arasında bu konuda anlamlı fark görülmedi. Sadece 1 hasta % 50 fazla kilo kaybını yakalayamadı. 55 yaşındaki bu diyabetik hasta, ameliyattan sonraki 10. ayda (SADI-200) % 64 kilo kaybı gösterdi. Ancak, geçirdiği bir myokard infarktüsünden sonra fiziksel aktiviteyi azaltması söylendi ve hafif kilo alımı yaşandı. Bununla birlikte, antidiabetik tedaviyi bıraktı ve kan şekerleri tamamen normale döndü.
3 vaka (% 3) , ameliyattan sonraki 6 ay antidiabetik tedavi kullanmaya devam etti. Bunlardan ilki uzun süredir (30 yıl) ağır diyabetikti. Neredeyse saptanamayan düzeyde C-peptidi vardı ve düzensiz olarak kendi başına düşük doz (8 U) insülin kullanıyordu. İkinci vaka bir nakilli böbrek vakasıydı. Kortikosteroid ve immunoterapi alıyordu. Üçüncü hasta ise BMI değeri 33, C peptid değeri 0.4 olan bir kadındı. Son 30 yıldır günde 150 üniteden fazla insülin gerektiren şeker hastalığı vardı. Ameliyattan sonraki 8. ayda insülin gereksinimi 25 üniteye düşmüştü.
Diyabetik hastaların postoperatif ortalama kan şekeri düzeyi ilk yıl 94.7, ikinci yıl 93.1, 3. yıl 91.09 ve 4. yıl 79.6 idi. HbA1c değerleri ise sırasıyla 5.3, 5.2, 5.4 ve 5 oldu. İlk postoperatif yılda sadece 1 hastanın HbA1c düzeyi 6.5'in üstünde, 7 hastada ise 6-6.5 arasındaydı. Bunlarda 4'ü takip süresinde bu değerleri korudular.
Konsensus önerilerine göre, sağlanan düzelme oranı % 92 idi ve bu 49 hastanın 45'i 1 yıldan uzun süreyle takip edildi. Daha yüksek preoperatif HbA1c seviyelerine sahip hastalar anlamlı olarak daha yüksek kan şekeri, daha yüksek HbA1c ve daha yüksek trigliserid seviyelerine ve anlamlı düzeyde daha düşük BMI değerlerine sahiptiler.
Kan şekerinin yanısıra lipid metabolizması da ameliyat sonrasında ciddi şekilde düzeldi. Sadece % 27 hastada trigliserid düzeyleri yüksek kaldı, % 27'de HDL düzeyleri düşüktü, % 5 hastada LDL düzeyleri yüksekti ve sadece % 4 hasta yüksek kolesterol düzeylerine sahipti.
İki hasta direngen hipoalbuminemi nedeniyle revizyonel cerrahi gerektirdi. Bu iki hastada SADI-200, 3 m beslenme kanalı ve 2 m ortak kanal olacak şekilde Roux-en-Y duodenal switche çevrildi. Ortalama defekasyon sayısı günde 2.5 idi. Hipertansiyon hastaların % 98'inde kontrol altına alındı. % 58 hastada ise kesin iyileme sağlandı. Uyku apnesi hastaların % 88'inde tamamen düzeldi.
Tartışma:
4 yıldan uzun süre önce, morbid obezite ve metabolik komplikasyonlarını tedavi etmek üzere SADI-S ameliyatı geliştirilmiştir. (8,9) Bu modifikasyon, daha önceki başarılı operasyonlar temelinde malabsorbtif prensipleri koruyarak, ameliyatın karmaşıklığını, teknik zorluğunu ve cerrahi komplikasyon oranlarını azaltmak amacıyla geliştirilmiştir. (12-14) Yeterli bir kilo kaybı öngörülmüştür, çünkü ameliyatın kısıtlayıcı komponenti bir sleeve gastrektomidir ve intestinal bypass mini-gastrik bypasstakinden daha uzundur. (15) Bu nedenle, kilo kaybı ve ko-morbiditelerde düzelme anlamında SADI-S tatminkar sonuçlar oluşturacaktı. En önemli endişeler ise olası malnutrisyon ve afferent loopa reflüye bağlı potansiyel kilo geri alımıydı.
Başlangıçtan itibaren kilo kaybı oramları mükemmeldir. İlk 6 ayda erişilen fazla kilo kaybı oranı % 80'dir ve 18 aylık periodda % 100'e yaklaşmaktadır. Bu veri tüm takip süresince elde edilmiştir ve tüm diğer bariatrik prosedürlerden anlamlı şekilde yüksektir. (17) BPD'nin daha önceki versiyonları, orjinal Scopinaro prosedürü ve BPD-DS uzun vadede (10 yıldan fazla) % 70-80 EWL sunarlar. (18-20) Hess'in çalışmasına göre (19) maksimum kilo kaybı 3. postoperatif yılda sağlanır, sonra hastalar hafifçe kilo alır ve uzun vadede ortalama % 75 EWL düzeyinde bir plato sergilerler.
Bizim hastalarımız postoperatif dönemde daha büyük oranda kilo kaybetmiştir. Bu, daha fazla gastrik kısıtlanmaya bağlı olabilir. Protein ve nişasta emilimi SADI-S ve BPD-DS'de benzerdir. Çünkü beslenme kanalının uzunluğu tamamen aynıdır. SADI-S ile daha fazla yağ emilimi beklenebilir, çünkü ortak kanal daha uzundur. Bu henüz gözlemlenmemiştir ancak hastalarımızda tuvalete çıkma sayısı anlamlı olarak daha azdır. (2.3'e karşı 3.2) (19) Bu durum, daha düşük miktarda safra tuzunun kolona ulaşması ile açıklanabilir. (12)
BPD'nin her türünden sonra protein malnutrisyonu en önemli endişedir. Bu komplikasyonun net mekanizması Scopinaro tarafından kesin şekilde tariflenmiştir. (18) Ortak kanal uzunluğu 200 cm olan ilk 50 vakada klinik hipoalbuminemi oranı % 8 idi. Bu 4 hastanın 22si Roux-en-Y DS ile revizyona gittiler. Bu hipoalbuminemi oranını yüksek bulduğumuz için, ortak kanal uzunluğunu 250 cm'e çıkarmaya karar verdik. Son izlemlerde, SADI-S 250 vakalarında ciddi bir problem gözlenmedi. Şu anda, hasta seçimini de daha dikkatli yapıyoruz. Çünkü, bariatrik cerrahiden sonra protein malnutrisyonu gelişmesinden sorumlu temel faktör diyete uyumsuzluktur. (18) Bu nedenle, anormal diyet alışkanlıkları olan hastalar, emosyonel bozukluğu olanlar ve azalmış emilim kapasitesi nedeniyle çok ileri yaşlardakileri SADI-S uygulamak için kabul etmiyoruz.
Uzun vadede kilo geri alımı olasılığı hala mevcuttur. Afferent loopa reflü ve intestinal adaptasyon bunun sorumlusu olabilir. Çünkü, geçmişte jejunoileal bypass uygulanan hastalarda hastaların küçük bir bölümünde bu gözlenmiştir. Bununla birlikte, minigastrik bypass uygulanan hastaların uzun süreli takipleri, kilo geri alımının 1-loop rekonstrüksiyonla ilişkili olmadığını düşündürmektedir. (15,21)
SADI-S, bariatrik ameliyatlardan sonra Tip 2 diyabetin düzelmesinde etkili kanıtlanmış mekanizmaların çoğunu biraraya getirir. (22,23) Tip-2 diyabetli hastalarda sağlanan mükemmel sonuçlar, ameliyatın teknik olarak basitliği ve düşük komplikasyon oranlarıyla birleştirilince, metabolik hastalığı tedavi etmek için çok uygun bir seçenek olarak görünmektedir.
Roux-en-Y prosedürlerinden sonra beklenen internal herni oranları değişken olmakla birlikte, % 1 ile 16 arasındadır. (24,25) 1-loop rekonstrüksiyonlarından sonra bu oran neredeyse sıfırlanmaktadır. (21) Postoperatif internal hernilerin ortalama gözlenme zamanı 12 aydır. Hastaların % 80'inde 20 aydan önce görülür. Serimizde hiçbir internal herni vakası yoktur.
Tartışma:
Günümüzde morbid obezite veya ağır metabolik hastalıkları tedavi etmek üzere ideal olan tek bir çözüm yoktur. SADI-S tekniği süpermorbid hastalar ve anlamlı metabolik hastalığı olanlar için uygun bir operasyon olarak görünmektedir. Anastomoz yeri değiştirilerek hastaya adapte edilebilir. Bacak uzunluğu arttırılırsa sonuçları mini gastrik bypass gibi olmakla birlikte, 1-loop rekonstrüksiyon avantajlarını safra reflüsü olmadan sunmaktadır. Aksine, kısaltılırsa operasyon bu kez klasik BPD gibi davranmaktadır.
www.medicorium.com kaynak gösterilmeden ve link eklenmeden alıntı yapılamaz.
Andrés Sánchez-Pernaute
Surgery for Obesity and Related Diseases xx (2012) xxx
Referanslar
[1] Søvik TT, Taha O, Aasheim ET, et al. Randomized clinical trial of laparoscopic gastric bypass versus laparoscopic duodenal switch for superobesity. Br J Surg 2010;97:1606.
[2] Prachand VN, Ward M, Alverdy JC. Duodenal switch provides su- perior resolution of metabolic comorbidities independent of weight loss in the super-obese (BMI ???? or ???? 50 kg/m2) compared with gastric bypass. J Gastrointest Surg 2010;14:21120.
[3] Søvik TT, Aasheim ET, Taha O, et al. Weight loss, cardiovascular risk factors, and quality of life after gastric bypass and duodenal switch: a randomized trial. Ann Intern Med 2011;155:28191.
[4] Topart P, Becouarn G, Ritz P. Comparative early outcomes of three laparoscopic bariatric procedures: sleeve gastrectomy, Roux-en-Y gastric bypass, and biliopancreatic diversion with duodenal switch. Surg Obes Relat Dis 2012;8:250 4.
[5] Buchwald H, Estok R, Fahrbach K, et al. Weight and type 2 diabetes after bariatric surgery: systematic review and meta-analysis. Am J Med 2009;122:248 56.
[6] Aasheim ET, Björkman S, Søvik TT, et al. Vitamin status after bariatric surgery: a randomized study of gastric bypass and duodenal switch. Am J Clin Nutr 2009;90:1522.
[7] Dolan K, Hatzifotis M, Newbury L, Lowe N, Fielding G. A clinical and nutritional comparison of biliopancreatic diversion with and without duodenal switch. Ann Surg 2004;240:516.
[8] Sánchez-Pernaute A, Rubio Herrera MA, Pérez-Aguirre E, et al. Proximal duodenal-ileal end-to-side bypass with sleeve gastrectomy: proposed technique. Obes Surg 2007;17:16148.
[9] Sánchez-Pernaute A, Herrera MA, Pérez-Aguirre ME, et al. Single anastomosis duodeno-ileal bypass with sleeve gastrectomy (SADI-S): one to three-year follow-up. Obes Surg 2010;20:17206.
[10] Sánchez-Pernaute A, Pérez-Aguirre E, Díez-Valladares L, et al. Right-angled stapled latero-lateral duodenojejunal anastomosis in the duodenal switch. Obes Surg 2005;15:7002.
[11] Dixon JB, Zimmet P, Alberti KG, Rubino F, on behalf of the Inter- national Diabetes Federation Taskforce on Epidemiology and Preven- tion. Bariatric surgery: an IDF statement for obese type 2 diabetes. Surg Obes Relat Dis 2011;7:43347.
[12] Scopinaro N, Adami GF, Marinari GM, et al. Biliopancreatic diver- sion. World J Surg 1998;22:936 46.
[13] Hess DS, Hess DW. Biliopancreatic diversion with a duodenal switch. Obes Surg 1998;8:26782.
[14] Marceau P, Biron S, Bourque RA, Potvin M, Hould FS, Simard S. Biliopancreatic diversion with a new type of gastrectomy. Obes Surg 1993;3:29 35.
[15] Rutledge R. The mini-gastric bypass: experience with the first 1,274 cases. Obes Surg 2001;11:27680.
[16] Mason EE, Ito C. Gastric bypass. Ann Surg 1969;170:32936.?
[17] Buchwald H, Avidor Y, Braunwald E, et al. Bariatric surgery: a systematic review and meta-analysis. JAMA 2004;292:172437.
[18] Scopinaro N. Biliopancreatic diversion: mechanisms of action and long-term results. Obes Surg 2006;16:6839.?
[19] Hess DS, Hess DW, Oakley RS. The biliopancreatic diversion with the duodenal switch: results beyond 10 years. Obes Surg 2005;15: 408 16.?
[20] Marceau P, Biron S, Hould FS, et al. Duodenal switch: long-term results. Obes Surg 2007;17:142130.?
[21] Lee WJ, Lee YC, Ser KH, Chen SC, Chen JC, Su YH. Revisional surgery for laparoscopic minigastric bypass. Surg Obes Relat Dis 2011;7:486 92.?
[22] Pories WJ, Swanson MS, MacDonald KG, et al. Who would have thought it? An operation proves to be the most effective therapy for adult-onset diabetes mellitus. Ann Surg 1995;222:33950.
?[23] Hickey MS, Pories WJ, MacDonald KG Jr, et al. A new paradigm for type 2 diabetes mellitus: could it be a disease of the foregut? Ann Surg 1998;227:63743.
?[24] Rodríguez A, Mosti M, Sierra M, et al. Small bowel obstruction after antecolic and antegastric laparoscopic Roux-en-Y gastric bypass: could the incidence be reduced? Obes Surg 2010;20:1380 4.?
[25] Higa K, Ho T, Tercero F, Yunus T, Boone KB. Laparoscopic Roux- en-Y gastric bypass: 10-year follow-up. Surg Obes Relat Dis 2011; 7:516 25.